当地时间1月30日,国际顶级医学期刊《柳叶刀》在线发表最新论文,揭示新型冠状病毒(2019-nCoV)的基因组序列与SARS-CoV的差异很大,可以被认为是一种新型的人类感染性乙型冠状病毒。不过该病毒的原始宿主与SARS-CoV相同,都是蝙蝠。
同时,论文发现新型冠状病毒进入人类细胞所使用的分子“通道”,即人类的受体,可能也与SARS病毒相同,都是血管紧张素转化酶2(ACE2)。
值得注意的是,论文还披露了4个细节:
第一,疫情的首次报告是在2019年12月下旬,此时武汉的大多数蝙蝠都在冬眠。
第二,在华南海鲜市场上未发现有蝙蝠或出售蝙蝠,但是有许多包括哺乳动物在内的非水生动物。
第三,2019-nCoV与它的近亲bat-SL-CoVZC45和bat-SL-CoVZXC21 之间的基因序列相似度不到90%,这意味着这两种源于蝙蝠的冠状病毒并不是2019-nCoV的直接祖先。
第四,在SARS和MERS中,蝙蝠都是其自然宿主,另一种动物作为中间宿主,而人类作为最终宿主。
该研究在取自患者的全部10份基因样本中均发现了2019-nCoV,包括8个完整基因组和2个部分基因组。各样本的基因序列几乎完全相同(超过99.98%的基因序列相同),这表明该病毒是最近才侵染人类。
论文通讯作者之一、山东第一医科大学、山东省高等学校新发传染病病因流行病学实验室史卫峰教授表示,“值得关注的是,本研究发现来自不同患者的2019-nCoV病毒基因序列几乎相同。这一发现说明,分离得到的2019-nCoV起源于同一来源,传播发生的时间还很短,并被相对迅速地检测出来。但是,随着病毒传播给更多的人,对突变的发生进行不断的监测是有必要的。”
该论文来自中国疾病预防控制中心、山东大学、山东第一医科大学和山东医学科学院、湖北省疾病预防控制中心、深圳华大因源医药科技有限公司、中国科学院、解放军总医院、温州医科大学、悉尼大学、山东第一医科大学附属第一医院的研究人员。
样本采自9人,1人住海鲜市场附近酒店
论文从9名住院患者的支气管肺泡灌洗液和培养分离物样品进行了测序。
研究者表示,对这些2019-nCoV基因组和其他冠状病毒基因组进行的系统进化分析是为了确定该病毒的进化史,同时帮助推断其可能的起源。为了探索病毒可能的受体结合特性,研究者进行了同源性建模。
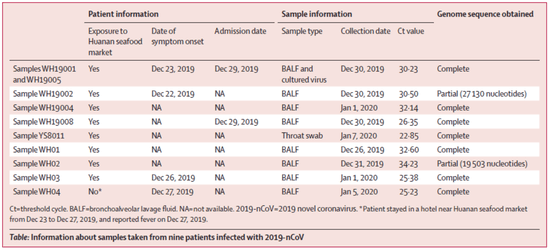
九名感染了2019新型冠状病毒的患者的样本信息
9名患者患有病毒性肺炎,并且常见呼吸道病原体呈阴性,去了至少三家位于武汉的医院就诊。他们中的8人在出现症状之前去过华南海鲜市场,另一人(WH04)没有去过市场,但于2019年12月23日至12月27日住在市场附近的酒店。
9人中的5人(WH19001、WH19002、WH19004、WH19008、YS8011)的样本由中国疾控中心(CDC)收集,CDC对样本进行测试,均对所有筛查的常见呼吸道病原体呈阴性。
其余4名患者(WH01、WH02、WH03、WH04)的样本由华大基因采集,检测结果显示对常见呼吸道病原体也均为阴性。
通过分析9名患者的样本,研究者获得了2019-nCoV的8个完整的和2个部分的基因组序列。
这些数据已保存在中国国家微生物数据中心(登录号NMDC10013002,基因组登录号NMDC60013002-01至NMDC60013002-10),而华大基因的数据已保存在中国国家基因库(登录号CNA0007332–35)。
基于这些基因组,研究者开发了一种实时PCR分析方法,并再次测试了华大基因的原始临床样品(WH01,WH02,WH03和WH04),以确定其阈值循环(Ct)值。其余样品通过中国疾病预防控制中心开发的另一种实时荧光定量PCR检测,Ct值范围为22.85至32.41。
这些结果证实了患者体内存在2019-nCoV。
病毒是最近才侵染人类,在遗传上与SARS-CoV不同
研究者从9名患者获取的10组2019-nCoV基因组序列高度相似,表现出超过99.98%的序列同源性性。而作为一种典型的RNA病毒,冠状病毒的平均进化速率约为每个位点每年10⁴个核苷酸取代,每个复制周期都会产生突变。
研究者们认为,这表明该病毒最近才出现在人类群体中。
对2019-nCoV完整基因组进行的源序列搜索则显示,GenBank(美国国家生物技术信息中心建立的DNA序列数据库)中最紧密相关的病毒是bat-SL-CoVZC45(同源性87.99%;查询覆盖率99%),以及另一种蝙蝠起源的SARS样乙型冠状病毒bat-SL-CoVZXC21(登录号MG772934;同源性87.23%;查询覆盖率98%)。这两种最紧密相关的病毒均采集于2018年中国东部城市舟山。
在五个基因区域(E,M,7,N和14)中,序列同源性大于90%,在E基因中最高(98.7%)。2019-nCoV的S基因与bat-SL-CoVZC45和bat-SL-CoVZXC21的序列同源性最低,仅为75%左右。另外,1b中的序列同源性(约86%)低于1a中的序列同源性性(约90%)。
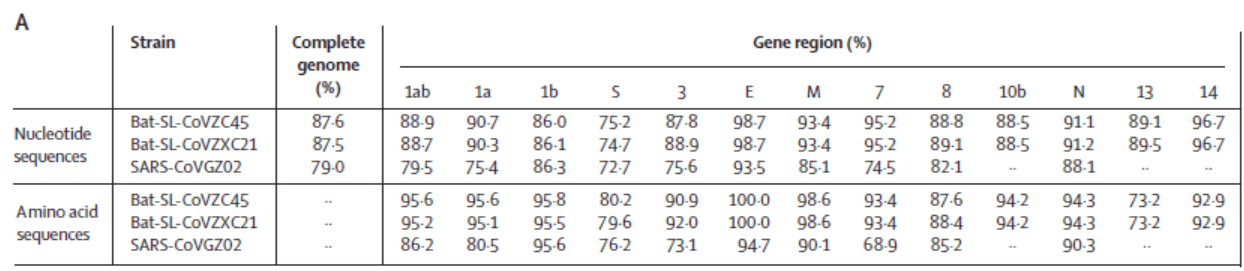 2019-nCoV与SARS-CoV GZ02(SARS冠状病毒,检索号AY390556)和蝙蝠SARS样冠状病毒bat-SL-CoVZC45(MG772933)和bat-SL-CoVZXC21(MG772934)的序列同一性
2019-nCoV与SARS-CoV GZ02(SARS冠状病毒,检索号AY390556)和蝙蝠SARS样冠状病毒bat-SL-CoVZC45(MG772933)和bat-SL-CoVZXC21(MG772934)的序列同一性
大多数编码蛋白在2019-nCoV和相关的蝙蝠衍生冠状病毒之间显示出高度的序列同源性(见上图)。不过,一个值得注意的例外是刺突蛋白,仅具有约80%的序列同源性。
与前述最紧密相关的两者相比,2019-nCoV与SARS-CoV(SARS冠状病毒,同源性约79%)和MERS-CoV(中东呼吸综合征冠状病毒,同源性约50%)的距离更远。
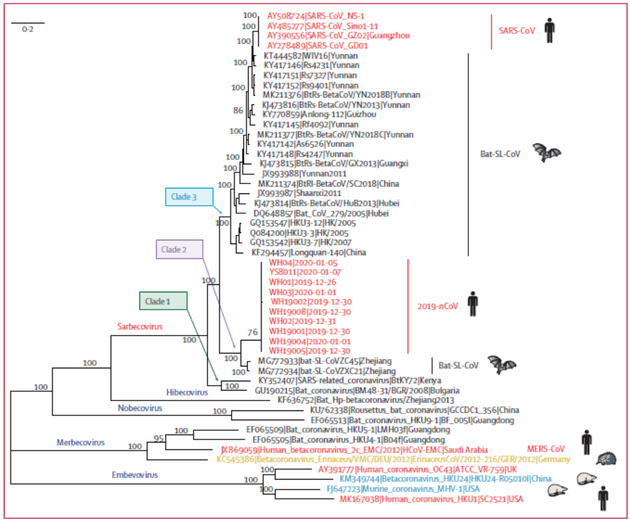
针对2019-nCoV和乙型冠状病毒属代表性病毒的全长基因组的系统发育分析
系统发育分析表明,2019-nCoV属于乙型冠状病毒Sarbecovirus亚属,与其最接近的bat-SL-CoVZC45和bat-SL-CoVZXC21的分支长度相对较长,并且在遗传上与SARS-CoV不同。
重要的是,同源性建模显示,2019-nCoV具有与SARS-CoV相似的受体结合域结构,尽管某些关键残基处存在氨基酸差异。
研究者们提到,2019-nCoV可能能够与人类的血管紧张素转化酶2(ACE2)受体结合,而血清ACE测定主要用于肺部疾病的诊断,对肝脏疾病、甲状腺疾病等其他系统疾病的诊疗也有一定价值。
蝙蝠进入冬眠,谁是中间宿主?
从流行病学角度来看,研究者研究的9名患者中有8名有接触武汉华南海鲜市场的历史,表明他们可能与市场上的感染源密切接触。但是有一名患者从未去过市场,尽管该患者在疾病发作之前住在市场附近的一家。这表明该患者可能由于飞沫传播染上病毒或被当前未知的来源感染。
目前可获得的数据表明,2019-nCoV病毒从蝙蝠库中感染了人类,但尚不清楚是否一种目前未知的动物充当了蝙蝠与人类之间的中间宿主。尽管研究者的系统发育分析也表明,蝙蝠可能是该病毒的原始宿主,但武汉华南海鲜市场上出售的一种动物可能是促使该病毒在人体内出现的中间宿主。
研究者们强调,一些事实表明:另一种动物正在充当蝙蝠与人类之间的中间宿主。
首先,该病毒暴发于2019年12月下旬首次被报道,当时武汉大多数蝙蝠物种正在冬眠。
其次,在华南海鲜市场上没有出售或发现蝙蝠,而有各种非水生动物(包括哺乳动物)可供购买。
第三,2019-nCoV与其近亲bat-SL-CoVZC45和bat-SL-CoVZXC21之间的序列同源性小于90%,因此,bat-SL-CoVZC45和bat-SL-CoVZXC21不是2019-nCoV的直接祖先。
第四,从此前研究结果来看,在SARS-CoV和MERS-CoV中,蝙蝠都是天然的病毒库(病毒来源),而另一只动物(SARS-CoV的果子狸和MERS-CoV的单峰骆驼)则作为中间宿主,人类是末端宿主。
因此,根据目前的数据,研究者认为造成武汉疫情爆发的2019-nCoV病毒似乎也可能最初是由蝙蝠作为宿主的,并且可能已经通过在华南海鲜市场出售的目前未知的某种或多种野生动物传播给了人类。